Choisir la bonne colonne pour la sélectivité chromatographique

Lors du développement d'une méthode pour l'analyse multirésidus de routine des pesticides dans les denrées alimentaires, plusieurs facteurs doivent être pris en compte lors du choix de la colonne de chromatographie liquide (CL) à utiliser. Ces exigences sont les suivantes
- Bonne rétention pour une gamme de propriétés physiochimiques (polaire, non polaire, base, acide).
- Résolution modérée à élevée (capacité maximale).
- Les extraits d'échantillons peuvent être bruts, la colonne doit donc avoir une stabilité mécanique.
- Bonne forme de pic pour une large gamme d'analytes.
- Capacité à transférer la séparation vers plusieurs instruments au sein du laboratoire et vers d'autres laboratoires.
Dans un blog précédent, nous avons décrit l'importance de la rétention, comment la calculer et faire en sorte que vos méthodes en aient suffisamment pour respecter les directives et donner des résultats fiables. Dans ce blog, je vais examiner certains paramètres de la phase stationnaire de la colonne et de la phase mobile qui peuvent avoir un impact sur la sélectivité des méthodes de chromatographie.
Lorsque l'on considère les différents facteurs d'une colonne de chromatographie liquide qui peuvent avoir un impact sur la sélectivité de la méthode, on peut les décrire comme des facteurs chimiques, comme indiqué ci-dessous :
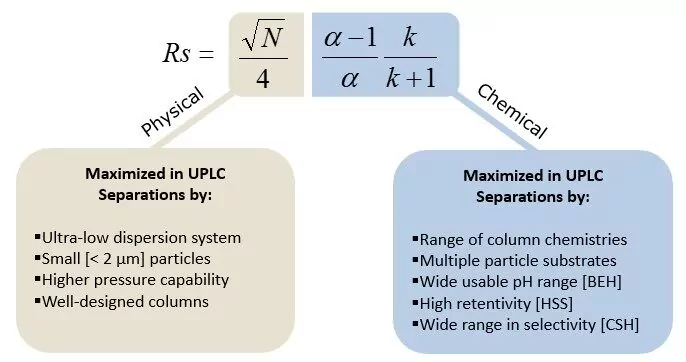
Qu'est-ce que la sélectivité ?
La sélectivité (α), est la capacité d'une méthode à distinguer deux analytes ou plus, elle peut être impactée par le choix de la phase stationnaire et des solvants et additifs de la phase mobile.
Un exemple de cas où la sélectivité peut être importante est celui des composés qui sont des isomères structurels tels que la sébuthylazine et la terbuthylazine. Si la séparation de ces deux composés n'est pas réalisée par notre méthode de chromatographie liquide, la méthode d'acquisition par spectrométrie de masse ne sera pas en mesure de distinguer les deux composés s'ils coéluent.
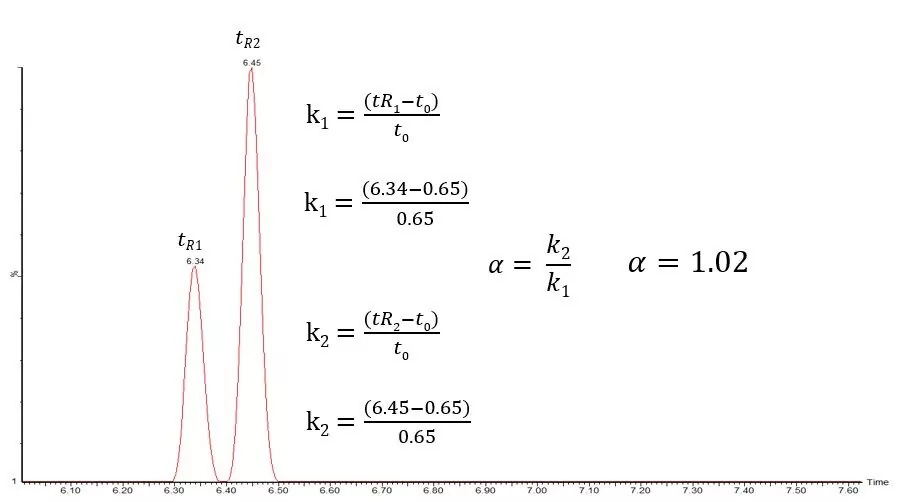
Pour calculer la sélectivité, nous devons connaître deux ou trois choses. Nous avons d'abord besoin du t0, que nous avons expliqué comment calculer dans le blog précédent. Nous avons également besoin des temps de rétention (tR1 et tR2) de nos deux composés d'intérêt. Une fois que nous avons rassemblé ces informations, nous pouvons utiliser l'équation suivante pour calculer le facteur de rétention (k) pour chacun de nos pics d'intérêt :
k = (tR - t0)/ t0
Calcul du facteur de rétention (k)
Une fois que nous avons nos valeursK1 et K2, nous pouvons alors calculer la sélectivité (α) entre nos deux pics en utilisant l'équation suivante qui donne un rapport des deux facteurs de rétention :
α = k2/k1
Calcul de la sélectivité (α), rapport du facteur de rétention (K) entre deux pics.
Si nous prenons la sebuthylazine et la terbuthylazine et que nous calculons le α en fonction de la séparation indiquée ci-dessous, nous obtenons un résultat de 1,02, la valeur augmentera si la séparation entre les deux pics est améliorée ou diminuera si les pics éluent plus près l'un de l'autre.
Facteurs influençant la sélectivité ?
En modifiant soit la phase stationnaire, soit la phase mobile, nous changeons la façon dont nos analytes interagissent entre ces deux phases. Si nos composés d'intérêt interagissent différemment avec ces deux phases, nous serons en mesure de les séparer, plus la différence est grande, plus la séparation est importante. Ceci est mesuré par le facteur de rétention (k) et nous pouvons mesurer les effets des changements de sélectivité entre les analytes en utilisant le facteur de sélectivité (α). Dans ce blog, nous nous concentrerons sur l'impact du changement de phase stationnaire sur la sélectivité ainsi que sur le rôle des solvants organiques. Dans un prochain blog, nous aborderons la manière dont l'utilisation d'additifs de phase mobile et de tampons affecte la sélectivité.
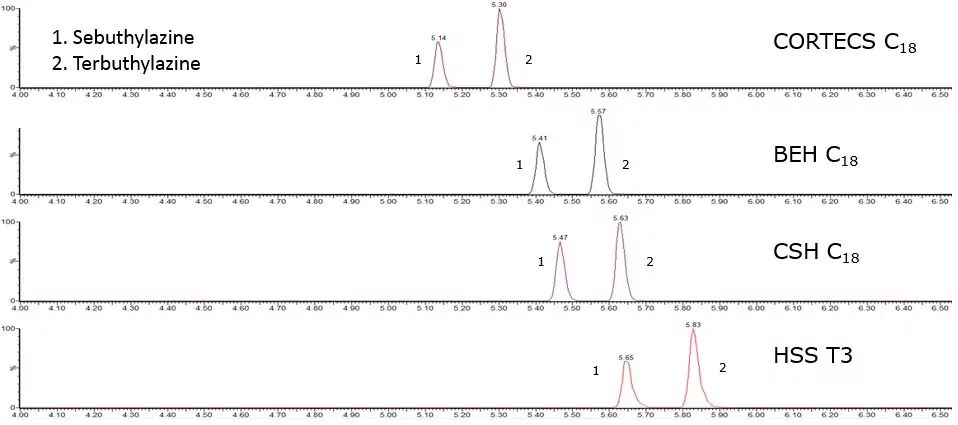
The use of C18 columns is common practice for the retention and separation of different pesticide classes in multiresidue methods. There are many different types of C18 columns and there will be retention and selectivity differences between them, depending on the ligand and base particles used. In the example below four different <2 µm Waters C18 stationary phases with the same dimensions (2.1 x 100 mm), have been tested using the same system and mobile phase to monitor the separation of sebuthylazine and terbuthylazine. These four C18 columns have a range of different characteristics which give them unique selectivity’s. The CORTECS C18 is a solid core 1.6 µm particle, providing high efficiency separations. The other three columns are fully porous particles, they include an ethylene bridged hybrid (BEH) C18, a charged surface hybrid (CSH) C18 and finally a high strength silica (HSS) T3 column. The HSS T3 column is a C18 stationary phase technology with proprietary end-capping, optimised pore size and ligand density to achieve optimum characteristics suited for polar compound retention under reversed phase conditions.

Le choix du solvant organique en chromatographie liquide en phase inversée peut produire des résultats différents lors de l'analyse de composés sur la même colonne. Les solvants courants tels que le méthanol et l'acétonitrile donnent des résultats différents et les propriétés de ces solvants doivent être prises en compte lors de l'élaboration d'une méthode. Le méthanol est un solvant protique, en raison du groupe hydroxyle (-OH), tandis que l'acétonitrile est le plus fort des deux solvants en termes d'élution en phase inversée, c'est aussi un solvant aprotique car il n'a pas d'atome d'hydrogène lié à un oxygène ou à un azote.
Dans le cas de nos deux isomères, l'utilisation de l'acétonitrile à la place du méthanol a eu un impact sur notre séparation de deux manières. Initialement, comme prévu, les pics ont été élués plus rapidement, ce qui n'est pas surprenant et attendu, l'acétonitrile étant le solvant d'élution le plus puissant. Dans ce cas cependant, l'acétonitrile a également donné une meilleure sélectivité entre les deux composés que celle observée avec le méthanol.
Conclusion
Les différentes phases stationnaires des colonnes et les solvants organiques sont des facteurs chimiques qui peuvent affecter la sélectivité et la résolution chromatographique. Même des colonnes différentes, classées C18, peuvent avoir des caractéristiques de rétention et de sélectivité différentes selon la particule de base et les ligands utilisés. Dans l'analyse des pesticides multi-résidus, on peut s'attendre à un certain compromis sur la performance chromatographique pour analyser une large gamme de composés ayant des propriétés physico-chimiques différentes. En effectuant des tests initiaux sur la phase stationnaire de la colonne et sur le solvant organique, il est possible d'évaluer des facteurs tels que la rétention, les séparations clés et la forme des pics afin de garantir l'obtention d'une performance chromatographique maximale, ce qui a un impact positif sur la qualité des données.
Sources d'information :
Sujets populaires
ACQUITY QDa (17) bioanalysis (11) biologics (14) biopharma (26) biopharmaceutical (36) biotherapeutics (17) case study (17) chromatography (14) data integrity (22) food analysis (12) HPLC (15) LC-MS (22) liquid chromatography (LC) (20) mass detection (16) mass spectrometry (MS) (54) method development (13) STEM (12) sustainability (12)


