Tests de dépistage néonatal de deuxième niveau - Améliorer la spécificité de l'une des plus grandes réalisations en matière de santé publique

Le dépistage néonatal des troubles héréditaires a été présenté comme l'une des dix plus grandes réalisations de la première décennie du XXIe siècle en matière de santé publique.1
La capacité d'identifier de manière pré-symptomatique les nouveau-nés susceptibles de développer des troubles endocriniens, hématologiques et métaboliques a considérablement amélioré ou sauvé des milliers de vies (et fait économiser des millions de dollars au système de santé) depuis que le premier test d'inhibition bactérienne du Dr Robert Guthrie a été utilisé pour dépister la phénylcétonurie (PCU) chez les nouveau-nés. Aujourd'hui, l'impact positif des programmes nationaux de dépistage néonatal est incontesté.
À l'instar du test du Dr Guthrie pour la PCU, le principal objectif de tous les tests de dépistage néonatals est de dépister rapidement et à moindre coût l'ensemble de la population desservie de nouveau-nés peu après la naissance. Ces tests sont des tests de dépistage et doivent avoir un haut degré de sensibilité diagnostique afin de ne pas manquer des bébés qui ont réellement un trouble. Dans la recherche de la plus grande sensibilité possible, certains tests de dépistage primaire des nouveau-nés souffrent d'une spécificité diagnostique moins que souhaitable, ce qui entraîne un certain nombre de résultats faussement positifs (des bébés identifiés comme risquant d'être atteints d'une maladie qui, en fin de compte, ne le sont pas). Il s'agit d'une décision consciente prise par la communauté du dépistage néonatal, car le préjudice résultant de l'absence de diagnostic dépasse de loin les préjudices potentiels associés à la génération d'une "fausse alerte".
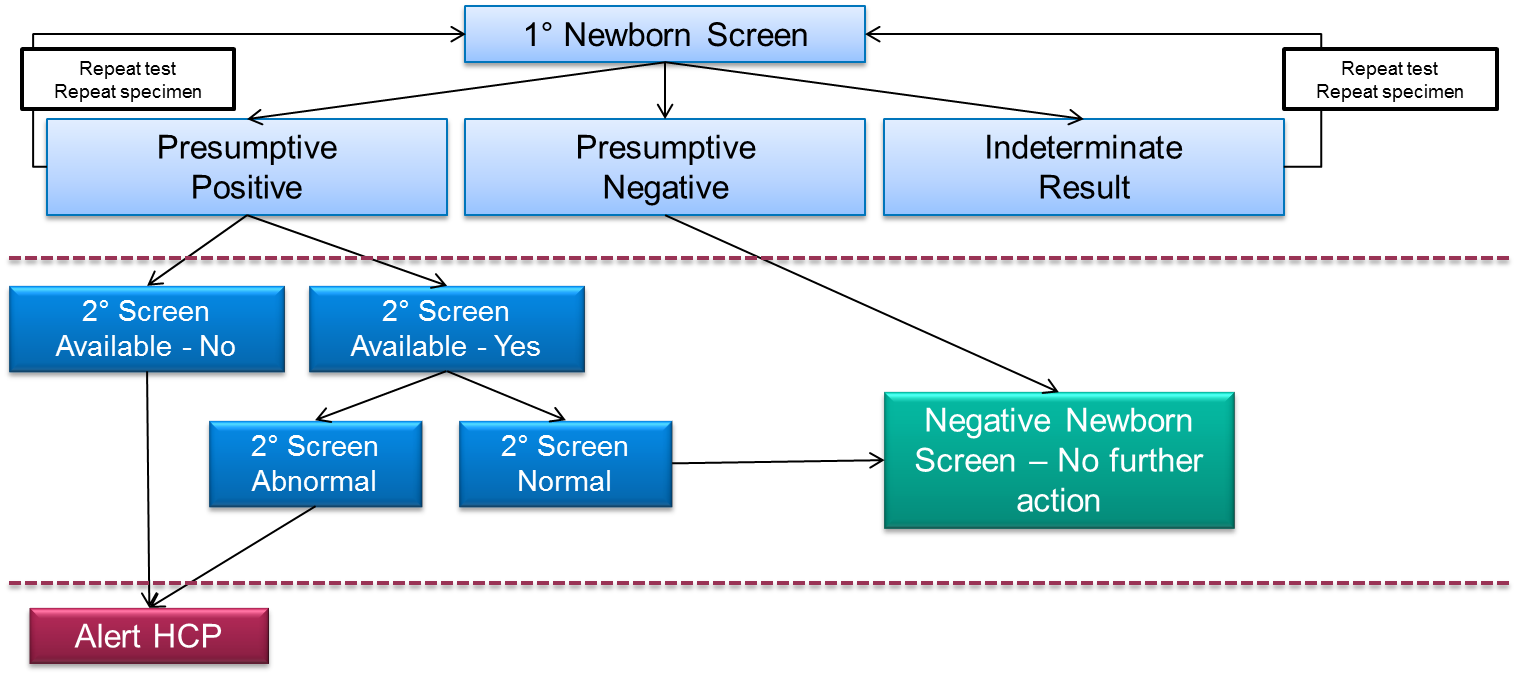
Figure 1. Exemple d'arbre de décision pour le dépistage néonatal lorsqu'un test de dépistage de deuxième niveau est disponible. Les mêmes échantillons qui sont positifs lors du test de dépistage primaire sont dirigés vers un test de dépistage de deuxième niveau (qui est souvent basé sur la LC-MS/MS) ayant un degré de spécificité diagnostique plus élevé. L'objectif de ces tests est de fournir des informations supplémentaires sur l'échantillon qui permettent au laboratoire de porter un jugement plus précis sur le risque de maladie, ce qui devrait éliminer le suivi inutile de bébés non affectés...
Quoi qu'il en soit, les résultats faussement positifs causent des préjudices tels que l'anxiété des parents2 et des examens médicaux inutiles, avec les dépenses que cela implique. Ainsi, la communauté du dépistage néonatal tente de minimiser le nombre de résultats faussement positifs qu'elle produit. L'une des façons d'y parvenir est de proposer des tests de dépistage néonatal de deuxième niveau qui sont appliqués à tous les tests positifs résultant du dépistage néonatal primaire (figure 1). Le test de dépistage primaire pourrait être un système d'analyse par injection de flux basé sur la spectrométrie de masse (FIA-MS/MS), mais il pourrait également s'agir d'un immunodosage ou d'une autre plateforme technologique. Un test de deuxième niveau est un test supplémentaire qui est effectué sur un ou plusieurs nouveaux disques, perforés à partir de l'échantillon primaire de sang séché (en d'autres termes, un nouvel échantillon n'est pas prélevé sur le bébé).
De nombreux tests de dépistage primaire ont une valeur prédictive positive élevée, même sans recourir à un test de deuxième niveau. Pour ces analytes, un résultat de dépistage en dehors de la plage de référence du laboratoire est très probablement le signe de la présence de la maladie cible. Pour plusieurs autres analytes, cependant, un résultat positif du dépistage primaire est associé à un degré de confiance moindre. Pour ces analytes ou ces conditions, il existe une probabilité raisonnable que le dépistage positif n'aboutisse pas à un diagnostic de la maladie. Les tests de dépistage qui sont candidats à l'ajout d'un test de deuxième niveau sont généralement ceux dont la spécificité diagnostique ou analytique est faible, soit parce que le résultat anormal est associé à plusieurs maladies ou affections bénignes non ciblées, soit parce que la plateforme de dépistage primaire est incapable de distinguer l'analyte cible des diverses interférences.
Un exemple de test avec une interférence analytique est la détection des espèces de leucine isobares par FIA-MS/MS. L'absence de séparation LC de la leucine, de l'isoleucine et de l'alloisoleucine, et l'interférence isobare de l'hydroxyproline, signifient qu'un résultat élevé de "leucines" n'équivaut pas toujours au diagnostic de la maladie urinaire du sirop d'érable (une maladie métabolique héréditaire qui est la seule cause connue d'une alloisoleucine élevée). Le test de deuxième niveau idéal dans ce scénario est une technique de séparation qui résout et quantifie toutes les espèces de leucine isobares de l'échantillon de sang. Si l'alloisoleucine est indétectable et que les concentrations des autres acides aminés ramifiés ne sont pas remarquables dans le test de deuxième niveau, il est possible d'exclure le risque de MSUD et il n'est pas nécessaire de procéder à des analyses des acides aminés plasmatiques et des acides organiques urinaires.
Un exemple de résultat de test ayant une faible valeur prédictive positive en raison d'une faible spécificité diagnostique est la découverte d'une élévation de la propionylcarnitine dans le test de dépistage primaire des acidémies propionique ou méthylmalonique. Une élévation de la proprionylcarnitine peut également être constatée chez les bébés nés de mères présentant une grave carence en vitamine B12. Lorsqu'un taux élevé de proprionylcarnitine est détecté par le dépistage par taches de sang séché, l'ajout d'une mesure de second niveau des acides organiques dans les taches de sang par LC-MS/MS3 peut rapidement révéler si le profil des métabolites suggère une maladie chez le nouveau-né (et dans ce cas, lequel des deux troubles est le plus probable), ou une carence en vitamines chez la mère. Dans le passé, la recherche d'un taux élevé de propionylcarnitine dans le sang déclenchait une série d'événements de suivi impliquant le rappel du bébé pour d'autres tests, ce qui était naturellement pénible pour la famille et épuisait les ressources du prestataire de services.
Un exemple de test pour lequel la spécificité analytique et diagnostique contribue à un taux élevé de faux positifs est le dosage immunologique par fluorescence de la 17-hydroxyprogestérone (17-OHP) sur sang séché dans le cadre du dépistage de l'hyperplasie congénitale des surrénales (HCS). La prématurité, le faible poids à la naissance et la détresse néonatale sont tous associés à une élévation transitoire de la 17-OHP, ainsi qu'à une multitude d'autres hormones stéroïdiennes structurellement apparentées, dont certaines peuvent présenter une réaction croisée avec les anticorps des immunodosages. L'analyse des stéroïdes surrénaliens par LC-MS/MS permet de distinguer le 17-OHP des autres hormones non associées à l'HCA. Elle permet également la quantification multiplexée du cortisol, de l'androsténédione et du 11- et 21-déoxycortisol, qui, lorsqu'ils sont combinés dans un calcul de ratio, peuvent prédire avec un degré de certitude plus élevé si l'élévation du 17-OHP est réellement associée à l'HCA ou si une autre condition bénigne est présente, qui ne nécessite pas de suivi.
Une analyse rétrospective de quatre années de données de dépistage de la Mayo Clinic du Minnesota a montré que l'introduction d'un test de deuxième niveau pour les stéroïdes surrénaliens après un dépistage primaire du 17-OHP par immunodosage n'a entraîné que 211 renvois, pour un coût total d'un peu plus de 270 000 dollars pour la clinique et le laboratoire. Si le test de deuxième niveau n'avait pas été mis en place, 2 712 cas auraient dû être suivis, pour un coût estimé à 2,3 millions de dollars. L'introduction du test de deuxième niveau basé sur le LC-MS/MS a permis de réduire les dépenses liées à la recherche de bébés non affectés de 8 dollars par naissance vivante à seulement 80 cents. Étant donné que le coût du dépistage néonatal au Minnesota est actuellement estimé à 101 dollars parcas5, cela représente un énorme gain d'efficacité. Des économies qui pourraient être réinvesties pour l'expansion future du dépistage.
Ressources :
-
- Dix grandes réalisations en matière de santé publique - États-Unis, 2001 - 2010.
- Schmidt, J.L. et al. The impact of false-positive newborn screening results on families : a qualitative study. doi : 10.1038/gim.2011.5.Genet Med. Jan;14(1):76-80. 2012.
- Monostori, P. et al. Détermination simultanée de l'acide 3-hydroxypropionique, de l'acide méthylmalonique et de l'acide méthylcitrique dans les taches de sang séché : Test LC-MS/MS de deuxième niveau pour le dépistage néonatal de l'acidémie propionique, des acidémies méthylmaloniques et des troubles de reméthylation combinés. PLoS ONE. Sept;12(9). https://doi.org/10.1371/journal.pone.0184897.2017.
- Matern, D. et al. Reduction of the false-positive rate in newborn screening by implementation of MS/MS-based second-tier tests : The Mayo Clinic experience. JIMD. Aug;30(4):585-592. 2007.
- Centre national de dépistage néonatal et de ressources mondiales: https://genes-r-us.uthscsa.edu/resources/consumer/statemap.htm. 3 novembre 2014.
En savoir plus sur le dépistage des nouveau-nés par spectrométrie de masse :
Sujets populaires
ACQUITY QDa (17) bioanalysis (11) biologics (14) biopharma (26) biopharmaceutical (36) biotherapeutics (17) case study (17) chromatography (14) data integrity (22) food analysis (12) HPLC (15) LC-MS (22) liquid chromatography (LC) (20) mass detection (16) mass spectrometry (MS) (54) method development (13) STEM (12) sustainability (12)